
肿瘤疫苗治疗和免疫治疗都是通过人体免疫系统杀伤癌细胞的新疗法,但是这两种治疗方法有着本质的区别,肿瘤疫苗是利用的抗原抗体反应,而免疫治疗则是针对的免疫检查点,因此,需要鉴别这两种方法就要从基本理念和作用机制进行剖析。
1
肿瘤疫苗是指通过将肿瘤组织中或者人体体液中提取的肿瘤相关抗原注射于肿瘤患者体内,激活机体免疫系统杀灭肿瘤细胞的特异性免疫反应,以达到控制和治疗肿瘤的目的。常见的肿瘤抗原有 MUC1,Wnt1,HER2,MART1,gp100 和酪氨酸酶等。
机体正常的免疫系统都能通过激活 T 细胞识别肿瘤细胞表面抗原,发生抗原抗体反应,从而杀伤肿瘤细胞(如图 1 所示),肿瘤疫苗是将该效应进一步强化,利用大剂量的肿瘤抗原刺激机体产生大量的针对某种肿瘤的抗体并通过抗原抗体免疫反应杀伤具有相同抗原的肿瘤细胞。
HER2/neu 肿瘤疫苗不但在乳腺癌治疗方面取得了较好的临床试验数据,而且在 HER2 表达阳性的胃肠肿瘤也证实能够安全、有效的控制肿瘤。
然而,在研究中发现乳腺癌疫苗会受到肿瘤微环境、抗原递呈细胞等因素的影响,仍然需要更多的研究去克服这些因素才能制备出更适合大众需要的乳腺癌疫苗。
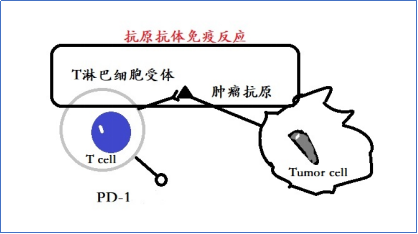
图 1 正常机体免疫反应通过激活的 T 细胞与肿瘤抗原发生免疫反应杀伤肿瘤细胞
2
免疫治疗又称免疫检查点治疗,是通过免疫检查点抑制剂抑制肿瘤免疫负调控机制来增强免疫细胞(细胞毒性 T 细胞)杀伤肿瘤细胞的能力,从而达到杀伤肿瘤细胞的目的。
免疫检查点是指减弱免疫细胞对癌细胞杀伤的免疫负调控信号,包括 PD-1、PD-L1 和 CTLA-4(如图 2 所示)。临床实践中应用的免疫检查点抑制剂,其中针对 PD-1 的有纳武单抗、帕博利珠单抗、卡瑞丽珠单抗等,针对 PD-L1 的有阿替利珠单抗、度伐利尤单抗等,针对 CTLA-4 的是伊匹单抗(Ipilimumab),同时也有更多的临床试验正在对新型的免疫检查点抑制剂进行相关临床研究。

图 2 肿瘤细胞表面 PD-L1 与 T 细胞表面 PD-1 结合避免免疫系统的识别与杀伤,CTLA-4 表达于效应 T 细胞表面负责传递抑制免疫信号
3
总而言之,肿瘤疫苗与免疫治疗具有共同的特点,但又具有不同的作用机制和作用位点,肿瘤疫苗是在多肽或蛋白质分子水平构建肿瘤抗原并激活效应 T 细胞产生抗肿瘤的抗原抗体免疫反应,免疫治疗是在免疫检查点分子水平上对各检查点进行抑制并恢复效应 T 细胞对肿瘤细胞的杀伤效能。
✩ 本文仅供医疗卫生等专业人士参考文中图片由作者提供策划:GoEun,梅浙投稿及合作:yinqihang@dxy.cn
题图来源:站酷海洛PLUS
参考文献
1. Saxena M, van der Burg SH, Melief CJM, Bhardwaj N. Therapeutic cancer vaccines. Nat Rev Cancer. 2021 Jun;21(6):360-378. doi: 10.1038/s41568-021-00346-0. Epub 2021 Apr 27. PMID: 33907315.
2. Brown TA 2nd, Mittendorf EA, Hale DF, Myers JW 3rd, Peace KM, Jackson DO, Greene JM, Vreeland TJ, Clifton GT, Ardavanis A, Litton JK, Shumway NM, Symanowski J, Murray JL, Ponniah S, Anastasopoulou EA, Pistamaltzian NF, Baxevanis CN, Perez SA, Papamichail M, Peoples GE. Prospective, randomized, single-blinded, multi-center phase II trial of two HER2 peptide vaccines, GP2 and AE37, in breast cancer patients to prevent recurrence. Breast Cancer Res Treat. 2020 Jun;181(2):391-401. doi: 10.1007/s10549-020-05638-x. Epub 2020 Apr 22. PMID: 32323103.
3. Mittendorf EA, Ardavanis A, Symanowski J, Murray JL, Shumway NM, Litton JK, Hale DF, Perez SA, Anastasopoulou EA, Pistamaltzian NF, Ponniah S, Baxevanis CN, von Hofe E, Papamichail M, Peoples GE. Primary analysis of a prospective, randomized, single-blinded phase II trial evaluating the HER2 peptide AE37 vaccine in breast cancer patients to prevent recurrence. Ann Oncol. 2016 Jul;27(7):1241-8. doi: 10.1093/annonc/mdw150. Epub 2016 Mar 30. PMID: 27029708.
4. McCarthy PM, Clifton GT, Vreeland TJ, Adams AM, O'Shea AE, Peoples GE. AE37: a HER2-targeted vaccine for the prevention of breast cancer recurrence. Expert Opin Investig Drugs. 2021 Jan;30(1):5-11. doi: 10.1080/13543784.2021.1849140. Epub 2020 Dec 3. PMID: 33191799.
5. Xu M, Kallinteris NL, von Hofe E. CD4+ T-cell activation for immunotherapy of malignancies using Ii-Key/MHC class II epitope hybrid vaccines. Vaccine. 2012 Apr 16;30(18):2805-10. doi: 10.1016/j.vaccine.2012.02.031. Epub 2012 Mar 3. PMID: 22386748.
6. Gordon B, Gadi VK. The Role of the Tumor Microenvironment in Developing Successful Therapeutic and Secondary Prophylactic Breast Cancer Vaccines. Vaccines (Basel). 2020 Sep 14;8(3):529. doi: 10.3390/vaccines8030529. PMID: 32937885; PMCID: PMC7565925.
7. Buonaguro L, Tagliamonte M. Selecting Target Antigens for Cancer Vaccine Development. Vaccines (Basel). 2020 Oct 17;8(4):615. doi: 10.3390/vaccines8040615. PMID: 33080888; PMCID: PMC7711972.
8. Basu A, Ramamoorthi G, Jia Y, Faughn J, Wiener D, Awshah S, Kodumudi K, Czerniecki BJ. Immunotherapy in breast cancer: Current status and future directions. Adv Cancer Res. 2019;143:295-349. doi: 10.1016/bs.acr.2019.03.006. Epub 2019 May 2. PMID: 31202361.
9. Sharma A, Subudhi SK, Blando J, Scutti J, Vence L, Wargo J, Allison JP, Ribas A, Sharma P. Anti-CTLA-4 Immunotherapy Does Not Deplete FOXP3+ Regulatory T Cells (Tregs) in Human Cancers. Clin Cancer Res. 2019 Feb 15;25(4):1233-1238. doi: 10.1158/1078-0432.CCR-18-0762. Epub 2018 Jul 27. PMID: 30054281; PMCID: PMC6348141.
10. Sharma A, Subudhi SK, Blando J, Vence L, Wargo J, Allison JP, Ribas A, Sharma P. Anti-CTLA-4 Immunotherapy Does Not Deplete FOXP3+ Regulatory T Cells (Tregs) in Human Cancers-Response. Clin Cancer Res. 2019 Jun 1;25(11):3469-3470. doi: 10.1158/1078-0432.CCR-19-0402. PMID: 31160495; PMCID: PMC6662573.
11. Mousavi-Niri N, Naseroleslami M, Hadjati J. Anti-regulatory T cell vaccines in immunotherapy: focusing on FoxP3 as target. Hum Vaccin Immunother. 2019;15(3):620-624. doi: 10.1080/21645515.2018.1545625. Epub 2019 Jan 30. PMID: 30633616; PMCID: PMC6605713.
12. Han Y, Liu D, Li L. PD-1/PD-L1 pathway: current researches in cancer. Am J Cancer Res. 2020 Mar 1;10(3):727-742. PMID: 32266087; PMCID: PMC7136921.
